Cinética viral durante el primer mes de tratamiento en pacientes con hepatitis crónica C genotipo 1
Joaquín Rodríguez Sánchez-Migallón., B. López Viedma S. de Aparato digestivo. Hospital General Universitario de Ciudad Real. C/Obispo Rafael Torija s/n. Ciudad Real (C. Real). CP. 13005. España. Tlf: 638 489 515/ 926278000 ext.77235. e-mail: joakinrodriguez@gmail.com
Referente al artículo: Hernández A, Domper F, León A et al; Cinética viral durante el primer mes de tratamiento en pacientes con hepatitis crónica C genotipo 1. Rev Esp Enferm Dig 2009; 101 (10): 671-679.
Autores: J. Rodríguez Sánchez-M, B. López Viedma.
Unidad de Aparato Digestivo. Hospital General Universitario de Ciudad Real.
El virus de la hepatitis C (VHC) es la causa más frecuente de hepatitis crónica en nuestro medio. Existen 180 millones de personas infectadas a lo largo de todo el mundo, alcanzando en España una prevalencia de hasta el 2%. Se considera la principal causa de muerte por enfermedades hepáticas, liderando la indicación de trasplante hepático en EEUU (1). Existen datos que avalan que la tasa de mortalidad por hepatitis C (por fallo hepático y hepatocarcinoma) seguirá aumentando en las dos próximas décadas (2).
La evolución natural de la Hepatitis por VHC es hacia la cronicidad en el 55-85% de los casos. De ellos, del 5% al 25% desarrollarán cirrosis hepática en un plazo de 20 a 30 años (3).
Existen 6 genotipos diferentes de VHC (G1 a G6) y cada uno se divide en subtipos designados por letras (ejemplo: G1a y G1b). La historia natural de la enfermedad es similar con todos los genotipos, pero la tasa de respuesta al tratamiento es del 38% al 52% para los genotipos 1 y 4, y del 90% para los genotipos 2 y 3.
El tratamiento combinado con Interferón pegilado alfa (Peg IFN) y Ribavirina (RBV) se considera de elección, a la espera de nuevas terapias en los próximos años. La elección de este régimen de tratamiento se realizó en base a los resultados publicados por tres ensayos que demostraban la superioridad de la pauta combinada con respecto al uso aislado de un fármaco u otro (4,5,6).
El tratamiento con Peg IFN + RBV es capaz de erradicar la infección en la mitad de los pacientes tratados, pero con una tasa importante de efectos secundarios, como: alteraciones del estado de ánimo, hipo-hipertiroidismo, citopenias, cuadro pseudogripal, etc, que lo cual empeora su calidad de vida (7). Los estudios sobre la cinética viral (variaciones de la carga viral durante el tratamiento medidas en UI/ml de ARN-VHC), han permitido establecer una serie de términos (tabla 1), que definen la respuesta al tratamiento y así poder confeccionar una serie de factores predictores de respuesta.
En el análisis de datos obtenidos en el estudio de acreditación del Peg IFN+ RBV, en pacientes naïve (aquellos que no han recibido nunca tratamiento), se observó un dato con alto valor predictivo negativo (VPN) de respuesta al tratamiento: si a las 12 semanas de recibir tratamiento la viremia no era negativa (EVR completa) o no había descendido al menos 2 logaritmos (EVR parcial), únicamente se podría esperar una respuesta sostenida (SVR) en el 3% de los pacientes tratados (7), y por tanto se aconsejaría la suspensión del tratamiento. Las recomendaciones actuales en el tratamiento del VHC contemplan la EVR como punto de decisión para los pacientes infectados con los genotipo 1 y 4, tratados durante 48 semanas, y se considera la retirada precoz del tratamiento en aquellos que no alcancen este criterio. Los genotipos 2 y 3, por el contrario no necesitan la determinación en la semana 12, dada su elevada tasa de respuesta obtenida en la semana 24.
Cuando la viremia es negativa a las 4 semanas, se denomina respuesta viral rápida (RVR), hecho de gran importancia, porque es capaz de predecir la SVR y modificar en función de ello las distintas pautas de duración del mismo.
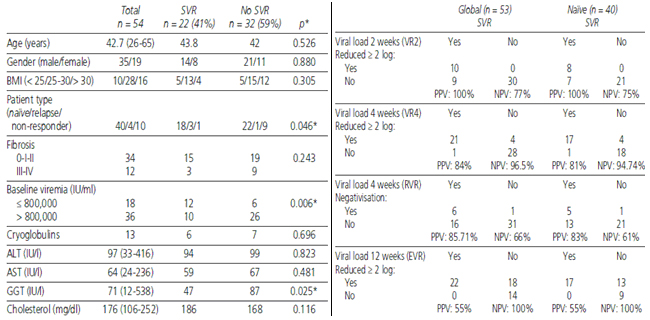
Referente a este concepto, Hernández y cols (9) elaboraron un estudio longitudinal, de seguimiento de una cohorte de 57 pacientes con hepatitis crónica VHC genotipo 1 remitidos a la consulta de hepatología del Hospital General Universitario de Ciudad Real entre enero de 2004 y octubre de 2006, donde se identificaron distintos factores predictores de respuesta al tratamiento con Peg IFN + RBV en relación con la respuesta viral sostenida (SVR), estudiando tanto factores basales (antes del inicio del tratamiento), como de la cinética viral en la semanas 2, 4 y 12 de tratamiento. El estudio alcanzó significación estadística (tabla 2) en la carga viral basal (p=0,006), GGT basal (p=0,025) y el tipo de paciente: naïve, recidiva, no respondedor (p=0,046). Aunque la mayor significación estadística se evidenció en el parámetro cinética viral (p=0,001) definido como el descenso de la carga viral >2 logaritmos en la semana 2 (RV2), semana 4 (RV4) y semana 12 (EVR). La RV2 tuvo un VPP del 100% que fue disminuyendo conforme avanzaba el tratamiento. Por el contrario, el VPN se fue incrementando hasta alcanzar el 100% en la semana 12 (RVP), por lo que una rápida respuesta, pronostica la curación, mientras que la falta de respuesta tras la semana 12, indica que el paciente será no respondedor (tabla 2). En el subanálisis realizado en el grupo de pacientes naïve, se hallaron los mismos resultados añadiendo el mayor índice de masa corporal (IMC) como factor predictor negativo de SRV (p=0,033).
A la luz de los resultados de este estudio, el descenso de la viremia >2 logaritmos a las 2 semanas de tratamiento (RV2) aseguró la SVR, por lo que estaría justificada la monitorización de la respuesta a este nivel. Dato que supondría la capacidad de predecir la efectividad del tratamiento de forma muy precoz, hecho que extrapolado a la práctica clínica conlleva una motivación extra en la adherencia al tratamiento por parte de los pacientes. Además se observó un alto VPN (alta probabilidad de no respuesta) en los pacientes que en la semana 4 no habían conseguido disminuir la viremia en dos logaritmos (RV4). Si este último dato se confirmara en otros estudios, avalaría la suspensión precoz del tratamiento en estos pacientes, evitando efectos secundarios y costes.
FIGURAS Y TABLAS:
BIBLIOGRAFÍA:
(1): Kim WR. The burden of hepatitis C in the United States. HEPATOLOGY 2002;36(Suppl):S30-S34.
(2): Deuffic-Burban S, Poynard T, Sulkowski MS, Wong JB. Estimating the
future health burden of chronic hepatitis C and human immunodeficiency virus infections in the United States. J Viral Hepat 2007;14:107-115.
(3): Seeff LB. Natural history of chronic hepatitis C. HEPATOLOGY 2002;36(Suppl):S35-S46.
(4): Manns MP, McHutchison JG, Gordon SC, Rustgi VK, Shiffman M, Reindollar R, et al. Peginterferon alfa-2b plus ribavirin compared with interferon alfa-2b plus ribavirin for initial treatment of chronic hepatitis C: a randomised trial. Lancet 2001;358:958-965.
(5): Fried MW,Shiffman ML, Reddy KR, Smith C, Marinos G, Goncales FL, Jr., et al. Peginterferon alfa-2a plus ribavirin for chronic hepatitis C virus infection. N Engl J Med 2002;347:975-982.
(6): Hadziyannis SJ, SetteHJr, Morgan TR, Balan V, Diago M, Marcellin P, et al. Peginterferon-alpha2a and ribavirin combination therapy in chronic hepatitis C: a randomized study of treatment duration and ribavirin dose. Ann Intern Med 2004;140:346-355.
(7): Aguilar J; dinámica viral y predicción de la respuesta al tratamiento con interferón pegilado y ribavirina en pacientes con hepatitis crónica por virus C. Rev Esp Enferm Dig 2009; 101: 665-670.
(8): Ghany MG, Strader DB, Thomas DL, Seeff LB; American Association for the Study of Liver Diseases. Diagnosis, management, and treatment of hepatitis C: an update. Hepatology. 2009 ;49: 1335-74.
(9): Hernández A, Domper F, León A et al; Cinética viral durante el primer més de tratamiento en pacientes con hepatitis crónica C genotipo 1. Rev Esp Enferm Dig 2009; 101 (10): 671-679.















Palabras Clave: cinética viral, factores predictores de respuesta, hepatitis C, respuesta viral sostenida